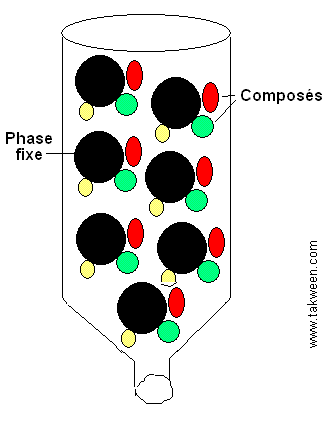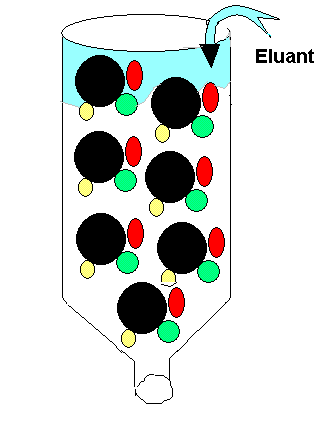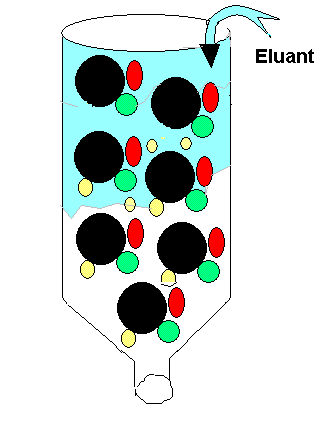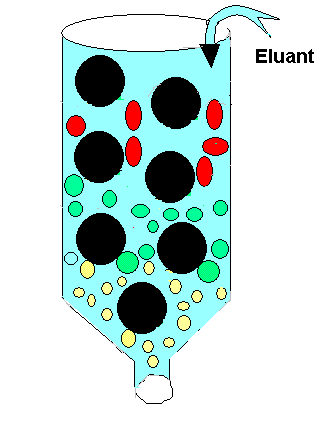
L'examen corrigé du module 'Techniques analyses' couvre la Centrifugation (séparation par densité/taille), la Spectrophotométrie (quantification via loi de Beer-Lambert (A = a x l x C), spectrophotométrie par mesure de l'absorbance/transmittance), et la Chromatographie (séparation par affinité fixe/mobile, ex: CCM, identification par Rf), des techniques fondamentales pour isoler, identifier et quantifier des molécules en biochimie. Application sur la quantification par spectrophotométrie des acides nucléiques (ADN, ARN). Ici examen contrôle du module 'techniques analyses', FSSM 2023.

Abonnement soutien takween ICI
EXEMPLES DE QCMs du CONTROLE 'TECHNIQUES D'ANALYSES' :
QUESTION 1. Aprés une centrifugation sous gradient de densité, les différents constituants du mélange se séparent dans le tube en fonction :
A- d'une densité croissante du bas en haut.
B- d'une densité croissante du haut en bas .
C- de leur polarité.
D- de leur charge électrique.
QUESTION 2. Le coefficient de sédimentation ne dépend pas de la :
A- densité de la particule.
B- masse de la particule.
C- forme de la particule.
D- vitesse de centrifugation.
QUESTION 3. La densité optique ou absorbance d'une radiation électromagnétique est définie comme étant:
A- le logarithme du rapport de l'intensité transmise et celle émise.
B- la différence entre l'intensité émise et l'intensité transmise.
C- le logarithme de la différence entre l'intensité émise et l’intensité transmise.
D- la différence du logarithme de l'intensité émise et du logarithme de l'intensité transmise.
.........................................
QUESTION 8. Une solution de cytosine montre une absorbance à 270 nm de 0,35 et une absorbance de 0,07 à 280 nm. Soit C270 la concentration déterminée en utilisant la D0 à 270nm et C280 la concentration déterminée en utilisant la D0 à 280 nm. La comparaison de ces deux résultats donnera :
A- C270 = 5 C280.
B- C270 = C280/5.
C- . C270 = C280.
D- C270 > 5 C280.
QUESTION 9. Une solution de cytosine montre une absorbance à 270 nm de 0,35 et une absorbance de 0,07 à 280 nm. Soit C270 la concentration déterminée en utilisant la D0 à 270nm et C280 la concentration déterminée en utilisant la D0 à 280 nm.
Les coefficients d'extinctions molaires de la cytosine déterminés à 270nm (Epsilon 270, ε270) et à 280nm (ε280) seraient:
A- ε270 = 5xε280.
B- ε270 = ε280/5.
C- ε270 = ε280.
D- ε270>5xε280.
QUESTION 10. Aprés dilution 10 fois, une solution aqueuse de tryptophane montre une absorbance dans l’UV à 280 nm de 0,16. La mesure directe de l'absorbance de la solution initiale (sans dilution) aurait donné une D0 de:
A- 1,6.
B- inférieure à 1,6.
C- supérieure à 1,6.
D- impossible à mesurer.
QUESTION 11. Le spectre d'absorption visible (400-700 nm) d'une solution aqueuse incolore de glycine pure présentera :
A- plusieurs pics d’absorbance.
B-un seul pic d'absorbance.
C- aucun pic d'absorbance.
D- un nombre de pics variable selon la concentration de la glycine.
.........................................
QUESTION 15. Le temps de rétention d'une substance est indépendant :
A- du volume de rétention.
B- du débit de la phase mobile.
C- de la taille de la colonne chromatographique.
D- du mélange dans lequel elle se trouve.
QUESTION 16. La substance à utiliser comme étalon interne doit être un composé :
A- majoritaire dans le mélange.
B- minoritaire dans le mélange.
C- non présent dans le mélange.
D- non identifié dans le mélange.
 |
 |
 |
EXEMPLES DE QCMs de L'EXAMEN CORRIGE du MODULE 'TECHNIQUES ANALYSES'. CENTRIFUGATION, SPECTROPHOTOMETRIE et CHROMATOGRAPHIE (suite):
Probléme I. ENONCE: Une extraction a été réalisée à partir de graines de sésame finement broyées par l'eau. L'extrait aqueux brut est réextrait par l’octane (C8H18). ll s'agit d'une extraction liquide- liquide à volumes égales d'octane et d'extrait aqueux.
QUESTION 17.
L'extrait aqueux a été mélangé a l’octane pour extraire les :
A- substances apolaires.
B- substances polaires.
C- substances insolubles dans l’extrait.
D- solubles dans l'eau.
Probléme I, suite (voir ENONCE de Q17).
QUESTION 18.
Lors de cette extraction, un coefficient de partage eau/octane donné sera spécifique à :
A- une seule substance donnée.
B- toutes les substances dans l'extrait.
C- toutes les substances extraites par l’octane.
D- toutes les substances solubles dans l’octane.
Probléme I, suite (voir ENONCE de Q17).
QUESTION 19.
Si l’extrait brut renferme différentes substances, celle dont la concentration sera la plus élevée dans l’octane est obligatoirement:
A- la plus soluble dans l'octane.
B- la plus concentrée dans l'extrait aqueux.
C- la moins soluble dans l'eau.
D- autre.
Probléme I, suite (voir ENONCE de Q17).
QUESTION 20.
Des macromolécules peuvent précipiter dans l'extrait aprés :
A- dilution.
B- centrifugation .
C- filtration.
D- acidification.
Probléme II. ENONCE: Lors d'une centrifugation à 15 000 tr/min utilisant un rotor de 30 cm de rayon, une protéine (P) a complètement sédimenté aprés avoir parcouru 10 cm dans le tube (soit 40 cm de l'axe de rotation).
QUESTION 21. En unités internationales, 1 Sv (Svedberg) est équivalent à :
A- 10 N.m.
B- 10-2 N.m-1.
C- 10 s.
D- 10-13 s.
.......................................................
Probléme II, suite (voir ENONCE de Q21).
QUESTION 22.
Quelle a été la vitesse angulaire (w) appliquée lors de cette centrifugation ?:
A- 1570 rad/s.
B- 3140 rad/s.
C- 250 rad/s.
D- 500 rad/s.
Probléme II, suite (voir ENONCE de Q21).
QUESTION 23.
Quelle a été la vitesse angulaire en unités internationales, (m/s) que subit cette protéine une fois sédimentée ? :
A- 628 m/s.
B- 1256 m/s.
C- 100 m/s.
D- 200 m/s.
Probléme II, suite (voir ENONCE de Q21).
QUESTION 24.
La force relative de centrifugation qu'a subie cette protéine au point final de sa sédimentation est :
A- 2600 g.
B- 8200 g.
C- 1006 g.
D- 4100 g.
Probléme II, suite (voir ENONCE de Q21).
QUESTION 25.
La protéine (P) est mélangée à des protéines étalons A, B et C dont les masses molaires respectives (en Da) sont 5000, 25000, 50000. Les volumes d'élutions respectifs de A, P, B et C sont égaux à 75 mL, 62 mL, 55 mL et 45 mL. Quelle serait, approximativement, la masse molaire de la protéine P (en Da)?;
A- 6025.
B- 7400.
C- 14000.
D- 23500.
Probléme III. ENONCE. On se propose de déterminer les concentrations d'ARN et D’ADN dans un extrait d'acides nucléiques débarrassé des protéines. Après dilution, cet extrait donne les absorbances suivantes : A260 = 0,874 et A280 = 0,460. Sachant que :
- L'ARN pur montre un rapport (A260/A280) = 2,1; alors que l'ADN pur donne un rapport (A260/A280) = 1,8
- Une concentration de 20 µg/mL d'ARN pur donne une absorbance à 260 nm A260 = 0,5, alors qu’il en faut 25 µg/mL d'ADN pour avoir la même absorbance à cette longueur d'onde.
QUESTION 26.
Avant élimination des protéines, l'extrait aura une :
A- absorbance nulle à 280 nm.
B- absorbance nulle à 260 nm.
C- absorbance plus importante à 260 nm.
D- absorbance moins importante à 280 nm.
.......................................................
Problème III, suite (voir ENONCE de la Q26).
QUESTION 29.
En examinant les absorbances de cet extrait on peut en déduire que le mélange contient:
A- 33% d'ARN.
B- 33% d'ADN.
C- 55% d'ARN.
D- 55% d’ADN.
Problème III, suite (voir ENONCE de la Q26).
QUESTION 30.
La concentration de l’ADN dans cet extrait est:
A- 26,90 µg/mL .
B- 13,44 µg/mL .
C- 22,18 pg/mL.
D- 18,15 µg/mL.
- Question 28: B.
Il y a dans cet extrait plus d'ADN que d'ARN (Réponse B). Voir figure Q28 (démonstration).

Question 29: C.
Le mélange contient environ 55 % d'ARN et 45 % d'ADN, car le rapport A260/A280 de l'échantillon est de 1,90 (0,874/0,460), ce qui se situe entre 1,8 (ADN pur) et 2,1 (ARN pur) et indique une proportion d'ARN supérieure à l'ADN, conduisant à la bonne réponse C) 55% d'ARN, en utilisant les facteurs de conversion pour calculer la concentration d'ARN et d'ADN.

Question 30: D.
La concentration d'ADN dans cet extrait est de 18,15 µg/mL (Option D), calculée en utilisant le système de deux équations basé sur les absorbances mesurées (A260 et A280) et les coefficients de conversion spécifiques à l'ADN et l'ARN fournis dans l'énoncé, résolvant ainsi pour la concentration d'ADN.

- Examen contrôle TP corrigé du module techniques analyses, FSSM, 2021
- Examen contrôle corrigé du module techniques analyses, FSSM, 2021
- Techniques d'Analyses en Biochimie
- Chromatographie
- Chromatographie couche mince, CCM
- Chromatographie d'affinité
- Chromatographie d'exclusion, gel filtration
- QCM Chromatographie, CCM
- Chromatographie, polarité
- spectrophotométrie. Exercices
Chaine
Youtube (abonnement). Plusieurs vidéos multilingues