
| French | Arabic | English |
| Liaison covalente | رابطة تساهمية | Covalent bond |
| Liaison ionique | رابطة أيونية | ionic bond |
| Liaison hydrophobe | رابطة تنافرية، رابطة هيدروفوبية | hydrophobic bond |
| Interaction hydrophobe | تفاعل هيدروفوبي | Hydrophobic interaction |
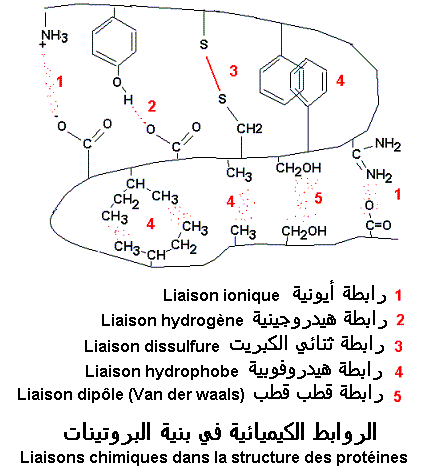
La plupart des fonctions de la cellules font intervenir des protéines. L'élucidation de leur mécanismes d'action nécessite la connaissance de leurs structures dont la structure primaire qui implique les liaisons chimiques contractées entre les acides aminés, comme la liaison ionique, liaison hydrogène, liaison de van der waals, liaison hydrophobe et les ponts dissulfures.
Faire les QCM d'abord et regarder plus de détails sur les réponses ensuite.
QUESTION 1. Choisir le(s) type(s) de liaisons chimiques correspondant à des liaisons fortes se formant quand des atomes adjacents ont en commun une ou plusieurs
paires d'électrons.
(L. covalentes)(!L. hydrogène)(!L.
de Van der Waals)(!L. ioniques)
QUESTION 2.
Choisir le type de liaison correspondant à des liaisons fortes qui se forment quand des ions de charges opposées s'attirent mutuellement.
(!L. covalentes)(!L. hydrogène)(!L.
de Van der Waals)(L. ioniques)
QUESTION 3.
Choisir le type de liaison correspondant à des liaisons faibles
se formant quand l'hydrogène d'une molécule polaire est attiré par un atome d'oxygène, d'azote ou de fluor.
(!L. covalentes)(L. hydrogène)(!L.
de Van der Waals)(!L. ioniques)
QUESTION 4. Choisir le type de liaison correspondant à des liaisons faibles qui se forment quand des molécules s'attirent entre elles.
Elles peuvent se former au sein d'une molécule ou entre des
molécules adjacentes.
(!L. covalentes)(!L. hydrogène)(L.
de Van der Waals)(!L. ioniques)
QUESTION 5.Quel est l'acide aminé incapable de former une liaison péptidique ? -cocher la réponse juste-: -
(Proline)(!Acide aspartique)(!Glycine)(!Phénylalanine)(!Lysine
)
QUESTION 6.Quel est l'état commun des Cystéines dans une protéine ?-cocher la réponse juste-: -
(!Etat sous forme 'ponts dissulfures')(Etat
sous forme thiol 'SH')
QUESTION 7.Les
protéines absorbent les rayons UV dans l'intervalle 275 à
290. Quels sont les acides aminés responsables de cette absorption
?-cocher la réponse juste-: -
(!Glycine, Serine)(Tryptophane,
Tyrosine, Phénylalanine)(!Valine, Proline,
Cystéine)(!Isoleucine, Leucine, Cystéine)(!Lysine,
Méthionine, Proline, Sérine)
QUESTION 8.Une
protéine à 4 Cystéines engagées toutes
dans des ponts dissulfures. Combien de structures protéiques
peuvent être formées ?-cocher la réponse juste-:
(!Deux)(Trois)(!Quatre)(!Cinq)(!Six)
QUESTION 9.Quels sont les types de liaisons qui peuvent être formées dans une protéine contenant, entre autres acides aminés, la Cystéine ? -cocher la réponse juste-: -
(!Liaison ionique, liaison de Van der Waals)(Ponts
dissulfures, liaison de Van der Waals)(!Liaison
hydrophobe, liaison de Van der Waals)(!Liaison
ionique, liaison hydrogène,liaison de Van der Waals )
QUESTION 10.Quels
sont les types de liaisons qui peuvent être formées dans
une protéine contenant, entre autres acides aminés,
la Lysine-cocher la réponse juste-: -
(Liaison ionique, liaison de Van der Waals)(!Ponts
dissulfures, liaison de Van der Waals)(!Liaison
hydrophobe, liaison de Van der Waals)(!Liaison
ionique, liaison hydrogène, liaison de Van der Waals)
QUESTION 11.Quels
sont les types de liaisons qui peuvent être formées dans
une protéine contenant, entre autres acides aminés,
l'Isoleucine-cocher la réponse juste-: -
(!Liaison ionique, liaison de Van der Waals)(!Ponts
dissulfures , liaison de Van der Waals)(Liaison
hydrophobe, liaison de Van der Waals)(!Liaison
ionique, liaison hydrogène, liaison de Van der Waals )
QUESTION 12.Quels
sont les types de liaisons qui peuvent être formées dans une protéine contenant, entre autres acides aminés, l'Acide glutamique-cocher la réponse juste-: -
(!Liaison ionique, liaison de Van der Waals)(!Ponts
dissulfures , liaison de Van der Waals)(!Liaison hydrophobe, liaison de Van der Waals)(Liaison ionique, liaison hydrogène, liaison de Van der Waals)
QUESTION 13.Combien
de liaisons peptidiques sont mises en jeu dans l'heptapeptide N-Ala-Trp-Ser-Pro-Leu-Ile-Gly-COOH?-cocher la réponse juste-: -
(!7 liaisons)(!6 liaisons)(5 liaisons)(!8 liaisons)
QUESTION 14.A
son point isoélectrique, une protéine présente:
-cocher la réponse juste-: -
(Une charge globale nette nulle)(!Souvent une solubilité élevée)(!Une charge électrique négative)(!Une charge électrique positive)
QUESTION 15.Quelles valeurs de pK marquées sur le schéma suivant, peut-on utiliser pour calculer le point isoélectrique de lacystéine ?: -cocher la réponse juste-: -

(!pK2 et pK3)(pK1 et pK3)(!pK1
et pK2)
QUESTION 16. Les 6 acides aminés ci dessous, ont un goût sucré résultant de leurs interactions avec les chaînes latérales des acides aminés des récepteurs du goût sucré, situés au niveau de la langue. Queles liaisons sont susceptibles d'être mises en jeu dans la détection du goût sucré ?: -cocher la réponse juste-: -
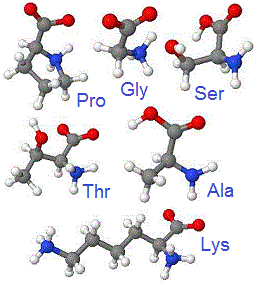
(!Liaisons hydrophobes, uniquement)(Liaison
hydrogène, uniquement)(!Liaisons de Van der Waals, uniquement)(Liaisons hydrogène et hydrophobes)
REPONSES. DETAILS

-
Explication question 5 :
PROLINE NE FORME PAS DE LIAISON PEPTIDIQUE
- Explication question 6 : CYSTEINES FORMENT DES PONTS DISSULFURE
- Explication question 7 : AC. AMINES A
STRUCTURE AROMATIQUE ABSORBENT LA LUMIERE A 280 nm
- Explication question 8 : 4 Cysteines
donnent 3 STRUCTURES AVEC PONTS DISSULFURE
- Explication question 9 : CYSTEINES:
PONTS DISSULFURE ET L. VANDER WAALS
- Explication question 10 : LYSINE: LIAISON
IONIQUE + L. VAN DER WAALS
- Explication question 11 : ISOLEUCINE:
LIAISON HYDROPHOBE + L. VAN DER WAALS
- Explication question 12 : ACIDE GLUTAMIQUE:
LIAISON IONIQUE + L. HYDROGENE + L. VAN DER WAALS
- Explication question 13 : HEPTAPEPTIDE:
5 LIAISONS, CAR PRO NE FORME PAS DE L. PEPTIDIQUE
- Explication question 14 : A SON PI, UNE
PROTEINE A UNE CHARGE ELECTRIQUE GLOBALE NULLE
- Explication question 15 : pI = (pK1 +pK3)/2, DISSOCIATION DANS L'ORDRE pK1 -> pK3 -> pK2, LA FORME A+- EST ENTOUREE PAR pK1 ET pK3
 |
 |
 |  |
LIENS UTILES:
- Liste des QCMs
- Examen contrôle corrigé du module 'Biochimie structurale', S3 (archives 2021)
- Structures of Amino acids. QCM
- Acides aminés, structure et propriétés. QCM
- Dosage des protéines. TP S3
- QCM Protéines (Structure)
- QCM fonction des protéines (Ar, Fr)
- Acides aminés. Ionisation (Exercices)
- Protéines, peptides (contrôles)
- Ionisation des acides aminés
- Autres
QCM Protéines, ADN, ARN
Takween. Supports
Chaine Youtube
(abonnement). Plusieurs vidéos multilingues


Enseignements par semestres
ANNONCES, INFORMATIONS
Congrès,
Conférences,...
- Congrès, Conférences
- Cours, Workshops
- Bourses, Postdocs
- Biotech-ecolo annonces
CONCOURS:
Concours de Pharmacie
الولوج إلى
الجامعة
ACCES A L'UNIVERSITE
تهييئ الانتقال من التعليم الثانوي إلى
التكوين الجامعي
Education. Preparation of the transition between Secondary and higher
levels (Préparation de la transition entre Enseignement secondaire
et Formation universitaire)
-
تحميل ملفات في مواضيع البيوكيمياء
Téléchargement de fichiers en Biochimie
Afin de pouvoir continuer à servir les visiteurs, soutenez nos actions sur le site takween en faisant acquisition des ouvrages et supports pédagogiques desitinés à améliorer l'enseignement et la recherche scientfique en Biochimie.
