
Le vivant contient un grand nombre de molécules organiques (جزيئات عضوية) et des molécules minérales (جزيئات معدنية) qui peuvent être sous différents états. Les molécules biologiques de base sont constituées de protéines, de glucides (sucres) de lipides et d'acides nucléiques. Elles constituent les bases en biochimie du vivant, Des liaisons chimiques (liaison hydrogène, liaison ionique, liaison hydrophobe) permettent l'édification de plusieurs molécules actives
يحتوي الكائن الحي على عدد كبير من الجزيئات العضوية والجزيئات المعدنية التي يمكن أن تكون في حالات مختلفة. تتكون الجزيئات البيولوجية الأساسية من البروتينات والكربوهيدرات (السكريات) والدهون والأحماض النووية. وهي تشكل قاعدة الحياة في الكيمياء الحيوية، الروابط الكيميائية (الرابطة الهيدروجينية، الرابطة الأيونية، الرابطة الكارهة للماء) تسمح ببناء عدة جزيئات نشيطة
SOMMAIRE
- AUTOASSOCIABILITE DES MOLECULES ET TENDANCE VERS LA COMPLEXATION
---- Molécules organiques (جزيئات عضوية) et molécules minétales (جزيئات معدنية). Exercices
---- QCM-liaisons
- 1. Forces électrostatiques
- 2. Forces de Van der waals
- 3. Liaisons hydrogène
- 4. Interactions hydrophobes
Matériaux BIOLOGIQUES DE BASE EN BIOCHIMIE
- 1. LIPIDES, DETERGENTS ET MEMBRANES BIOLOGIQUES
---- Exercices, QCM
- 2. OSES, OSIDES ET GLUCIDES
---- Exercices, QCM
- 3. ACIDES AMINES PEPTIDES ET Protéines
---- Exercices, QCM
- 4. BASES AZOTEES ET ACIDES NUCLEIQUES
---- Exercices, QCM
-- NUCLEOTIDE
-- DNA
-- RNA
ORGANISATION DES MOLECULES DANS LES CELLULES
---- Exercices, QCM
- 1. PAROI CELLULAIRE
- 2. MEMBRABE PLASMIQUE
- 3. CYTOPLASME
- 4. NOYAU CELLULAIRE
- 5. RETICULUM ENDOPLASMIQUE
- 6. APPAREIL DE GOLGI
- 7. MITOCHONDRIE
- 8. CHLOROPLASTE
- 9. INCLUSIONS, LYSOSOME ET PEROXYSOME
1. Quelles molécules dans les êtres vivants ?
1.1. Types de molécules dans les organismes vivants
---- 1.1.1. Molécules à l'état de gaz:
Les molécules à l'état de gaz correspondent aux molécules d'échange avec l'air lors du processus de la respiration. C'est le cas de l'oxygène (O2) qui est inspiré. Il traversera ensuite la membrane alvéolaire, le plasma sanguin, la membrane du globule rouge et finira par se fixer sur l'hémoglobine. Le gaz carbonique (CO2) sort du poumon lors de l'expiration. Dans les êtres vivants les molécules O2 et CO2 peuvent exister sous l'état dissous dans l'eau, s'ils ne sont pas combinés.
1.1.2. Molécules à l'état de solutions.
Plusieurs molécules des êtres vivants existent en solution dans les liquides biologiques comme le plasma sanguin, l'urine et le liquide céphalorachidien. Ces moleécules correspondent à des ions minéraux, des protéines (Matériaux-protéines), du glucose (Matériaux-glucides)...
Etant riche en macromolécules, le cytoplasme (cytosol) des cellules ne forme pas de vraies solutions transparente (solution non optiquement vide). Il est d'apparence visqueuse et s'écoule moins vite que l'eau. C'est une solution colloïdale
1.1.3. Ensembles moléculaires à l'état solide
Plusieurs ensembles moléculaires à l'état solides sont présents chez tous les êtres vivants. C'est
le cas des organites cellulaires comme les ribosomes,
les microtubules et les microfilaments. Des fibres extracellulaires sont présentes à l'état solides dans le tissu conjonctif. Certaines molécules existent même sous forme de cristaux. C'est le cas des cristaux de phosphate de calcium dans les os.
Molécules minérales
جزيئات معدنية
1.2.1. Métaux et métalloïdes
Les métalloïdes sont reconnus par leur position dans la classification périodique des éléments (table de Mendeliev). Ils occupent l'angle supérieur droit
(voir figure). Ils sont: C (carbone), N (azote), O
(oxygène), S (soufre), P (phosphore) et les
halogènes (F, Cl, Br, I). Tous les autres éléments
sont des métaux
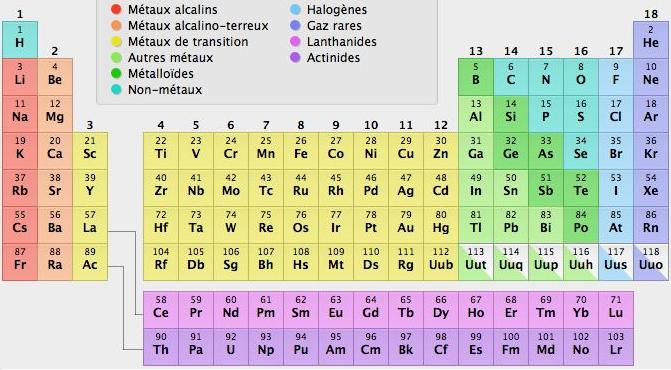
Les éléments d'une même famille (même colonne du tableau) possèdent des propriétés chimiques similaires et la place d'un élément dans la classification permet de prévoir ou d'expliquer ses propriétés chimiques.
Place
des métaux et des métalloïdes chez les êtres vivants
Métaux: Ca (1.90%), K (0.23%), Na (0.08%), Mg, Fe, Zn, Al, Cu, Mn, Pb, Se, Co, Mo (traces)
Métalloïdes: O (62,43%), C (21,15%), N (3.10%), P, S, Cl, I, F, Br, Si (inférieurs à 1%)
----- QCM éléments chimiques
REMARQUE: Le carbone (C) est un métalloïde qui peut être considéré élément minéral ou
organique (lorsqu'il échange au moins une liaison avec un autre atome de carbone ou un atome d'hydrogène). L'oxydation et l'hdratation du carbone donne un acide; l'acide carbonique (CO3H2).
Les métalloïdes et les métaux forment des corps différents une fois combinés avec l'oxygène et hydtatés
ensuite avec l'eau.
Les oxydes métalliques donnent des bases en se combinant avec l'eau. Ainsi, l'oxyde de sodium (Na2O) s'hydrate en soude (NaOH), l'oxyde de calcium (CaO)
s'hydrate en chaux (Ca(OH)2). (SO4H2), l'anhydride phosphorique (P2O5)
peut s'hydrater en acide orthophosphorique (PO4H3) (addition de 3 molécules d'eau), en acide pyrophosphorique (P2O7H4) (addition de 2 molécules d'eau) ou en acide méthaphosphorique (PO3H) (addition de 1molécules d'eau).
Les métaux sont des donneurs d'électrons (éléments électropositifs). Les métalloïdes sont des accepteurs d'électrons (élements électronégatifs).
Tous les éléments tendent à avoir la configuration des gaz inertes (dernière colonne droite de la classification) (règle de l'octet). Ainsi, certains atomes vont perdre (colonnes à gauche du tableau) ou gagner (colonnes à droite du tableau) des éléctrons pour devenir respectivement des cations (Na+, Mg++, ..) ou des anions (O--, S--, F-, Cl-,..).
Les oxydes métalloïques s'hydratent en acides. Ainsi, N2O3 s'hydrate en acide nitrique (NO3H), l'anhydride sulfurique (SO3) s'hydrate en acide sulfurique
Molécules organiques
جزيئات عضوية
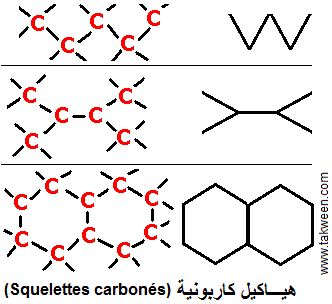
Squelette carboné الهيكل الكاربوني
L'ossature des molécules organiques est constituée d'atomes de carbone (C) qui peuvent former facilement des liaisons covalentes entre eux. C'est ce qu'on appelle le 'squelette carboné.

Les molécules organiques peuvent être linéaires ou cycliques. Elles peuvent être saturées (sans double liaisons) ou porteuses de doubles liaisons (insaturées).
Pour comprendre la structure d'une molécule organique, il est important de revenir à sa structure saturée probable et décrire les substitutions éventuelles des atomes d'hydrogène (H) par une ou plusieurs fonctions. Par exemple, le propoanol (CH3-CH2-OH) dérive d'un squelette à 3 carbones (propane) où un H a été substitué par un OH.
 |
 |
 |
 |
LIENS UTILES:
CONCOURS DE CHIRURGIE DENTAIRE
- Concours de pharmacie 2012
- Concours de pharmacie 2009
- Concours de pharmacie 2007 (Version Html)
- Concours de pharmacie 2007, complet. Version pdf
- Concours de Pharmacie 2006
- Autres concours (Biologie, Biochimie-Chimie, Physique, à partir de 2003) dans le livre 'Sciences de la vie. Protéines et Enzymes', Baaziz 2013 (+ DVD)
Takween. Supports
Chaine Youtube (abonnement). Plusieurs vidéos multilingues


Congrès,
Conférences,...
- Congrès, Conférences
- Cours, Workshops
- Bourses, Postdocs
- Biotech-ecolo annonces
-
تحميل ملفات في مواضيع البيوكيمياء
Téléchargement de fichiers en Biochimie